Định luật bảo toàn khối lượng là kiến thức cơ bản và vô cùng quan trọng mà học sinh cần nắm vững khi bắt đầu làm quen với môn hóa học. Hãy cùng chúng tôi tìm hiểu các kiến thức về định luật bảo toàn khối lượng trong bài viết này nhé!
Định luật bảo toàn khối lượng là gì?
Định luật bảo toàn khối lượng hay còn được biết đến với cái tên là định luật Lomonosov – Lavoisier, đây là định luật rất cơ bản trong lĩnh vực hóa học, định nghĩa như sau: Trong phản ứng hóa học, tổng khối lượng của các chất tham gia phản ứng sẽ bằng tổng khối lượng các sản phẩm tạo thành.
Nội dung định luật bảo toàn khối lượng
Để vận dụng một cách chính xác các công thức để giải các bài tập hóa học, chúng ta cần phải hiểu rõ bản chất cũng như nội dung của chúng.

Nội dung định luật bảo toàn khối lượng
Nội dung của định luật bảo toàn khối lượng như sau: Trong mỗi phản ứng hóa học đều có sự thay đổi liên kết giữa các nguyên tử, nhưng sự liên kết này chỉ liên quan tới các điện tử còn số nguyên tử của mỗi nguyên tố vẫn được giữ nguyên và khối lượng của các nguyên tử sẽ không có sự thay đổi. Do vậy mà tổng lượng của các chất vẫn được bảo toàn.
Định luật này còn có tên gọi khác đó là “định luật bảo toàn khối lượng của các chất”, bởi tại cùng một địa điểm thì trọng lượng sẽ tỷ lệ thuận với khối lượng. Lomonosov cũng nhận thấy, việc bảo toàn năng lượng có giá trị rất lớn với các phản ứng hóa học.
Ý nghĩa của định luật bảo toàn khối lượng: Trong các phản ứng hóa học, chỉ có điện tử thay đổi, còn số nguyên tử của nguyên tố sẽ được giữ nguyên và khối lượng của các nguyên tử cũng không thay đổi. Vậy nên khối lượng của các chất sẽ được bảo toàn.
Các hệ quả của của định luật bảo toàn khối lượng
Định luật bảo toàn khối lượng có hai hệ quả, đó là:
– Hệ quả 1: Trong mỗi phản ứng hóa học, tổng khối lượng của các chất trong phản ứng sẽ bằng với tổng khối lượng các chất thu được sau phản ứng. Theo đó, các chất thu được bao gồm những các sản phẩm hoặc có thể có cả các chất phản ứng còn dư.
– Hệ quả 2: Tổng khối lượng của các chất trong hỗn hợp sẽ bằng với tổng khối lượng các thành phần (nhóm nguyên tố hoặc nguyên tố) tạo ra các chất đó.
Cách tính định luật bảo toàn khối lượng
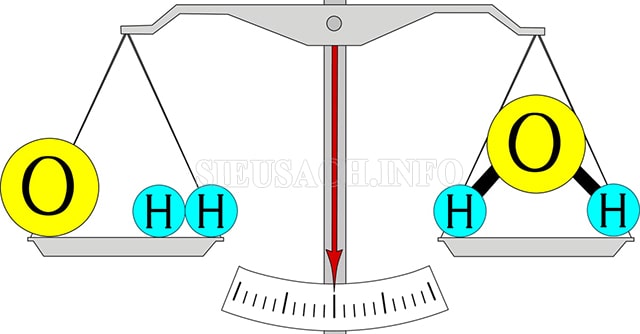
Công thức tính định luật bảo toàn khối lượng
Định luật bảo toàn khối lượng được tính như sau: Giả sử bạn có phản ứng giữa A + B sẽ tạo ra C + D, khi đó công thức sẽ được viết như sau:
mA + mB = mC + mD
Ví dụ thực tế: Bari clorua +natri sunphat tạo ra bari sunphat + natri clorua. Khi đó, chúng ta sẽ có công thức như sau:
mbari clorua + mnatri sunphat = mbari sunphat + mnatri clorua
Áp dụng định luật bảo toàn chúng ta có kết quả: Trong một phản ứng có n chất, nếu như biết khối lượng của (n – 1) chất thì chúng ta sẽ tính được khối lượng của chất còn lại.
Bài tập về định luật bảo toàn khối lượng
Bài tập 1: Có 10g canxi cacbonat (CaCO3) tạo ra 3,8 gam khí cacbonic (CO2) và x gam canxi oxit (CaO). Hãy viết phương trình phản ứng và tính khối lượng mà CaO được tạo thành qua phản ứng.
Đáp án:
Phương trình phản ứng: CaCO3 -> CaO + CO2
Trong phản ứng trên ta có 1 chất tham gia và tạo thành 2 sản phẩm mới.
Theo định luật ta có:
mCaCO3 = mCaO + mCO2
=> mCaO = mCaCO3 – mCO2 = 10 – 3,8 = 6,2g
Vậy khối lượng CaO tạo thành đó là 6,2g.

Bài tập áp dụng
Bài tập 2: Thí nghiệm Na2SO4 + BaCl2 -> BaSO4 + 2NaCl, sẽ cho ta biết khối lượng của Natri sunfat Na2SO4 là 14,2g. Trong khi đó, khối lượng của Natri Clorua NaCl và Bari sunfat BaSO4 và lần lượt là 11,7g và 23,3g. Hãy tính khối lượng Bari clorua BaCl2 đã tham gia vào phản ứng?
Giải:
Áp dụng định luật ta có:
mNa2SO4 + mBaCl2 = mBaSO4 + mNaCl
=> mBaCl2 = mBaSO4 + mNaCl – mNa2SO4 = 23,3 + 11,7 – 14,2 = 20,8g
Vậy khối lượng của BaCl2 tham gia phản ứng là 20,8g.
Bài viết trên đây đã giải thích định luật bảo toàn khối lượng. Hy vọng qua đây giúp bạn biết cách vận dụng để giải các bài tập khác nữa.




