Amoniac là gì? Amoniac có những tính chất hóa học, vật lý như thế nào? Bạn có đang thắc mắc ngoài những ứng dụng vốn có của amoniac thì chúng có gây hại gì cho sức khỏe hay không? Chúng ta sẽ cùng đi tìm hiểu trong bài viết dưới đây để hiểu hơn về chất hóa học này nhé.
Amoniac là gì?
Amoniac là cái tên được bắt nguồn từ tiếng Pháp là ammoniac và trong tiếng Việt được đọc là a-mô-ni-ắc. Đây là một hợp chất vô cơ được cấu tạo từ 3 nguyên tử Nitơ, 1 nguyên tử Hydro và tạo thành một liên kết kém bền vững, có công thức hóa học là NH3.
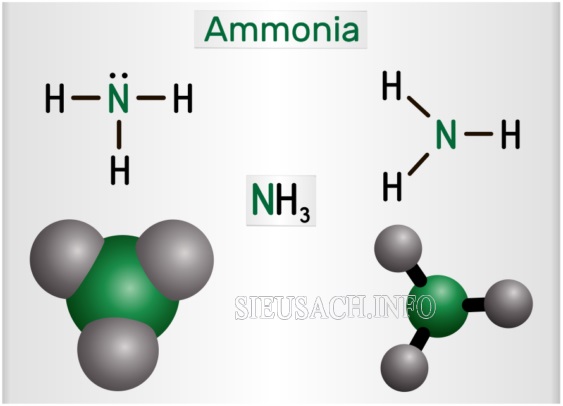
Amoniac là hợp chất vô cơ có nhiều trong tự nhiên
Mùi Amoniac là mùi gì?
Amoniac có mùi khai đặc trưng. Chúng ta có thể nhận biết mùi của Amoniac trong thành phần của nước tiểu bởi trong quá trình chuyển hóa thức ăn cơ thể người bài tiết ra một lượng Nitơ. Mặt khác, khi nitơ kết hợp với các chất hữu cơ khác dễ dàng tạo ra khí NH3.
Trong tự nhiên, NH3 được sinh ra rất nhiều. Ví dụ, trong thận của con người thường sản sinh ra một lượng nhỏ khí NH3. Chính vì vậy, chúng ta thường thấy nước tiểu sẽ có mùi khai đặc trưng giống như mùi của khí amoniac. Ngoài ra, khí amoniac còn được tạo ra bởi các sinh vật có trong tự nhiên trong quá trình phân hủy xác động vật.
Tính chất của amoniac là gì?
Cũng như những chất hóa học khác Amoniac (NH3) mang cả tính chất hóa học và tính chất vật lý. Cụ thể:
Tính chất vật lý Amoniac
- NH3 tồn tại ở dạng khí, không màu, có mùi hôi khai khó chịu. Nếu khí amoniac có nồng độ lớn có thể gây chết người.
- Amoniac có độ phân cực lớn bởi phân tử NH3 được tạo thành từ cặp electron tự do với liên kết N–H dễ bị phân cực; nên NH3 là chất dễ hóa lỏng.
- Dung dịch Amoniac là dung môi có khả năng hòa tan tốt trong: các dung môi hữu cơ do có hằng số điện môi nhỏ hơn nước. Đối với các kim loại kiềm và các kim loại Ca, Sr, Ba đều có thể hòa tan trong NH3 và tạo ra dung dịch có màu xanh thẫm.
- Khối lượng riêng của NH3 là 681 kg/m3 (ở nhiệt độ -33°C), dung dịch có tính bazo nên có độ pH > 12.

Amoniac có độ phân cực lớn
Tính chất hóa học Amoniac
- Amoniac thể hiện tính khử, kém bền bởi nhiệt nên nó dễ bị phân hủy ở nhiệt độ cao.
2NH3 → N2 + 3H2
N2 + 3H2 → 2NH3
- Amoniac tác dụng với ion kim loại, sau quá trình phản ứng tạo ra ion phức tạp.
2NH3 + Ag+ → [Ag(NH3)2]+
- Nguyên tử hidro trong amoniac dễ bị thay thế bởi các nguyên tử kim loại kiềm hoặc nhôm.
2NH3 + 2Na → 2NaNH2 + H2 (350 °C)
2NH3 + 2Al → 2AlN + 3H2 (800-900 °C)
- NH3 tác dụng với dung dịch muối: Dung dịch NH3 có khả năng tạo ra nhiều kết tủa dạng hidroxit kim loại khi tác dụng.
- Mang đặc điểm của một bazơ yếu nên dung dịch amoniac làm quỳ tím chuyển màu tím thành màu xanh. Do đó để có thể phát hiện ra dung dịch amoniac người dùng sẽ dùng quỳ tím ẩm để nhận biết.
- Amoniac tan trong nước, tác dụng với axit để tạo thành muối amoni.
Ứng dụng của amoniac trong đời sống, sản xuất công nghiệp
Amoniac được ứng dụng rộng rãi trong đời sống cũng như trong sản xuất công nghiệp. Dưới đây là một số ứng dụng điển hình của amoniac.
Phân bón
Thực tế amoniac lỏng được sử dụng đến khoảng 83% làm phân bón vì trong tất cả đều có hợp chất Nitơ có nguồn gốc từ NH3; là chất rất cần thiết cho sự phát triển của cây trồng.

NH3 được sử dụng làm phân bón cho cây trồng
NH3 và muối của nó được sử dụng như phân bón khi áp dụng cho đất, giúp tăng năng suất cho các loại cây trồng như lúa mì, ngô. Do đó, việc sản xuất amoniac đóng một thành phần quan trọng đối với ngân sách năng lượng thế giới.
Dùng làm thuốc tẩy
NH3 được sử dụng trong các hộ gia đình để tẩy rửa bề mặt như: thủy tinh, đồ sứ, thép không gỉ…
Trong ngành dệt may
Amoniac lỏng được sử dụng với nguyên liệu bông tạo ra một sản phẩm có khả năng kiềm bóng, sử dụng như chất kiềm. Đặc biệt chất này được sử dụng để chà rửa tiền bị lem.
Trong ngành công nghiệp thực phẩm
Amoniac thể hiện tính khử mạnh, trong ngành công nghiệp thực phẩm dung dịch amoniac được sử dụng để điều chỉnh độ chua. Bên cạnh đó, amoniac lỏng còn được dùng để giảm hay loại bỏ nhiễm khuẩn của thịt bò.
Xử lý môi trường khí thải
Amoniac lỏng ngày nay được sử dụng trong xử lý khí thải ra môi trường từ các nhà máy luyện gang thép, xi măng, lọc hóa dầu, nhiệt điện. Trong quá trình sản xuất các nhà máy này sẽ thải ra môi trường một lượng khí lớn các chất như: Nox, Sox.

NH3 giúp xử lý khí thải NOx, SOx ra môi trường
Khi đó người ta sẽ sử dụng NH3 làm chất khử trong nhiệt độ 300 – 450 độ C khi phản ứng hóa học với Nox sẽ tạo thành N2 và H2O đảm bảo giảm ô nhiễm.
Trong công nghiệp chế biến gỗ
Amoniac lỏng dùng trong ngành công nghiệp chế biến gỗ giúp cho màu sắc của gỗ tự nhiên đẹp hơn, đậm màu hơn.
Ngành công nghiệp dầu khí
Sử dụng Amoniac giúp trung hòa axit, các thành phần của dầu thô và bảo vệ các thiết bị khỏi bị ăn mòn.
Ngành công nghiệp khai thác mỏ
NH3 sử dụng để khai thác kim loại như: molypden, đồng niken từ quặng thiên nhiên.
Tác hại của Amoniac và cách xử lý khi khi bị nhiễm NH3
Tác hại của amoniac
Khí amoniac khi ở nồng độ đậm đặc sẽ gây nguy hiểm cho sức khỏe của con người. Cụ thể:
- Hít phải khí amoniac đậm đặc: gây bỏng niêm mạc mũi, rát cổ họng và đường hô hấp. Điều này làm ảnh hưởng, thậm chí nguy hiểm đến đường thở dẫn đến suy hô hấp vì NH3 có tính ăn mòn.
- Tiếp xúc trực tiếp: với da, mắt, phổi, hỏng sẽ gây bỏng nặng. Các vết bỏng này sẽ gây mù vĩnh viễn, các bệnh về viêm phổi, thậm chí tiếp xúc lượng lớn còn gây tử vong.
- Nuốt phải: Nếu vô tình nuốt phải amoniac đậm đặc gây bỏng miệng, họng, ruột, dạ dày nghiêm trọng.

Tác hại khi nuốt phải khí NH3
Các dấu hiệu bị nhiễm độc amoniac
Dưới đây là các dấu hiệu ngộ độc amoniac xảy ra khi hít, nuốt hoặc chạm vào lượng rất lớn các amoniac.
- Hô hấp: Ngực đau thắt, ho, khó thở, thở nhanh, thở khò khè.
- Mắt, miệng, họng: Đau họng nặng, đau miệng, chảy nước mắt và đốt mắt, mù mắt, môi sức.
- Tim mạch: Đập nhanh, mạch yếu, gây sốc phản vệ..
- Thần kinh: Gây chóng mặt, đi lại khó khăn, bị lẫn lộn, thiếu sự phối hợp, ngẩn ngơ, cảm thấy bồn chồn.
- Da: Môi, da có màu xanh lợt sẽ bị bỏng nặng nếu tiếp xúc lâu.
- Dạ dày và đường tiêu hóa: Có hiện tượng nôn, đau dạ dày nghiêm trọng.
Cách xử lý khi ngộ độc NH3
Dung dịch amoniac có nồng độ cao rất dễ gây độc cho con người. Tuy nhiên không phải ai cũng biết cách xử lý khi chẳng may tiếp xúc hay bị ngộ độc khí amoniac. Dưới đây là một số cách sơ cứu khi bị ngộ độc amoniac:
- Khi hít phải khí amoniac cần nhanh chóng chuyển nạn nhân đến nơi thoáng khí, cởi sạch quần áo đã bị dính amoniac.
- Cho bệnh nhân súc sạch miệng với nước sạch nếu bị nuốt phải amoniac sau đó cho uống tiếp 1-2 cốc sữa.
- Rửa tay với xà phòng và nước khi tiếp xúc với dung dịch NH3
- Nếu tiếp xúc với dung dịch amoniac dính trên da thì cần rửa sạch amoniac với xà phòng và rất nhiều nước.
- Nếu bị nặng cần phải đưa ngay nạn nhân đến trạm y tế hay bệnh viện để chữa trị kịp thời.
Trên đây là những chia sẻ về amoniac là gì, mùi amoniac là mùi gì, tính chất, ứng dụng và các tác hại của NH3. Mong rằng với những thông tin trong bài viết này sẽ mang đến cho bạn nhiều kiến thức hữu ích trong học tập cũng như trong cuộc sống.




