Bảng tính tan lớp 9 là phần kiến thức hóa học quan trọng mà học sinh cần nắm rõ để dễ dàng giải các bài tập nhanh và tốt hơn. Dưới đây chuthapdoquangninh.org.vn sẽ cung cấp các kiến thức về bảng tính tan hóa 9 và cách học nhanh bảng tính tan cực đơn giản.
Giới thiệu về bảng tính tan của các chất
Định nghĩa về độ tan là gì?
Độ tan là số lượng chất hóa học có thể tan trong dung môi nhất định ở điều kiện nhiệt độ, áp suất nhất định. Độ tan được biểu diễn dưới dạng phần trăm hoặc theo tỉ lệ khối lượng của chất hóa học tan trong đơn vị dung môi.
Độ tan là lượng chất hóa học có thể tan trong dung môi
Ví dụ: gam/lít, mol/lít, gram/100ml.
Muốn xác định độ tan của một chất trong nước thì ta có thể dựa vào cách xác định độ tan của chất trong 100g nước hòa tan có:
- Lớn hơn 10g chất tan thì đó là chất dễ tan hay còn gọi là chất tan nhiều.
- Nhỏ hơn 1g chất tan đó là chất tan ít, hay ít tan.
- Nhỏ hơn 0,01g chất tan thì đó là chất không tan.
Bảng tính tan là gì?
Bảng tính tan là một bảng gồm các hàng và các cột, với cột là các cation kim loại, còn hàng là các anion gốc axit (hay OH-). Đối với một chất cụ thể ta có thể xác định ion âm và ion dương, sau đó gióng theo hàng và cột tương ứng sẽ biết được trạng thái của chất đó tại một ô.
Ý nghĩa bảng tính tan lớp 9
Qua bảng tuần hoàn hóa học tính tan của các chất sẽ giúp các em học sinh hiểu rõ hơn về độ tan của chất, tính kết tủa, bay hơi của chất đó. Qua đó có thể giúp bài tập được giải quyết nhanh chóng hơn.
Ngoài ra, dựa vào bảng tính tan các em cũng có thể nhận biết được các chất trong phòng thí nghiệm nhanh chóng, đơn giản. Vì vậy, khi học hóa học thì bảng tính tan lớp 9 là phần kiến thức bắt buộc các em học sinh cần phải nhớ.
Cách sử dụng bảng tính tan trong học hóa
Trong bảng tính tan các em sẽ thấy bảng gồm các hàng và các cột, với:
- Các cột là các cation kim loại.
- Các hàng là các anion gốc axit (OH–).
Các ký hiệu trong bảng tính tan:
- T là tan
- K là không tan
- I là ít tan
- (-) là không tồn tại hoặc phân hủy
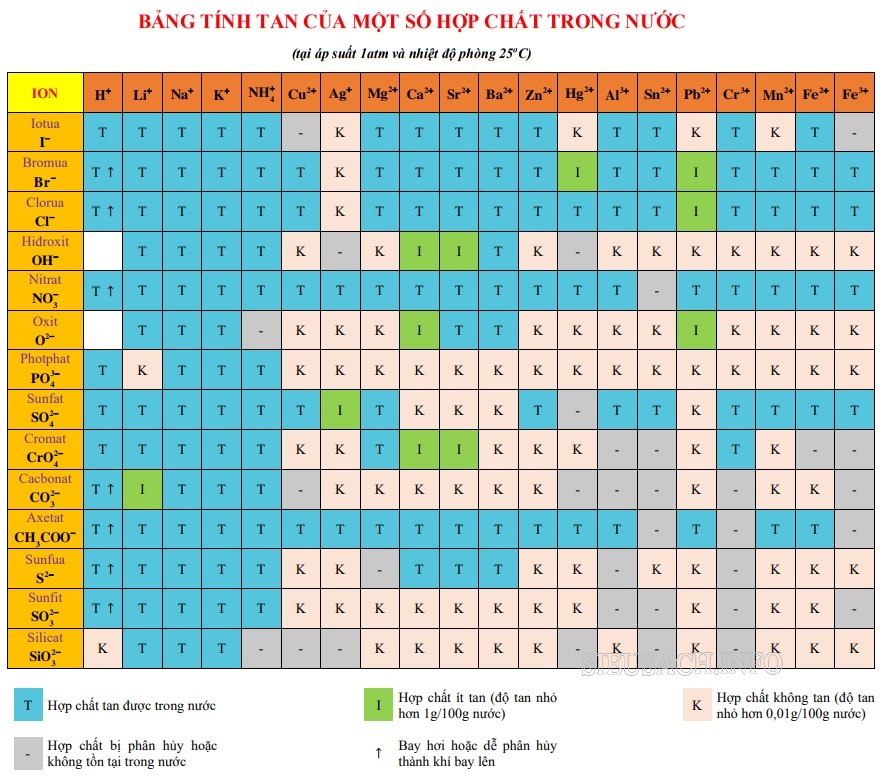
Bảng tính tan các chất trong hóa học
Khi nhìn vào bảng ta sẽ xác định được các ion âm, ion dương và sẽ xác định được trạng thái của chất đó ở dạng nào, tan hay không tan…
Ví dụ: Dựa vào bảng tính tan tìm AgCl là chất nào?
Ta có thể thấy trong bảng thì chất AgCl gồm có: ion Ag+ và ion Cl–, khi gióng cột và hàng của chúng thì ô đó thể hiện tính tan của AgCl. Theo đó, AgCl là chất không tan và tạo ra kết tủa màu trắng.
Mẹo cách học thuộc nhanh bảng tính tan lớp 9
Để ghi nhớ bảng tính tan nhanh và lâu thì làm nhiều bài tập là cách hiệu quả để các em học sinh có thể ghi nhớ kiến thức. Dưới đây, là mẹo học thuộc nhanh bảng tính tan cực nhanh và hiệu quả, chi tiết như sau:
Quy tắc rút gọn về tính tan cần nhớ
Dưới đây là một số quy tắc về tính tan mà các e cần ghi nhớ đơn giản như sau:
Tính tan đối với các muối
Hầu hết muối đều có gốc halogen, chẳng hạn muối: F, Cl, Br, I sẽ đều có khả năng tan trong nước. Tuy nhiên, khi cho Ag phản ứng với các nguyên tố này chúng sẽ không tan mà sẽ tạo ra kết tủa với màu đặc trưng.
Điều này rất hữu ích trong việc nhận biết các nguyên tố trong nhóm halogen. Như vậy, trong bảng tính toán về độ tan thì việc kết hợp bạc với Cl sẽ được ký hiệu là “k” – biểu thị không tan trong nước.
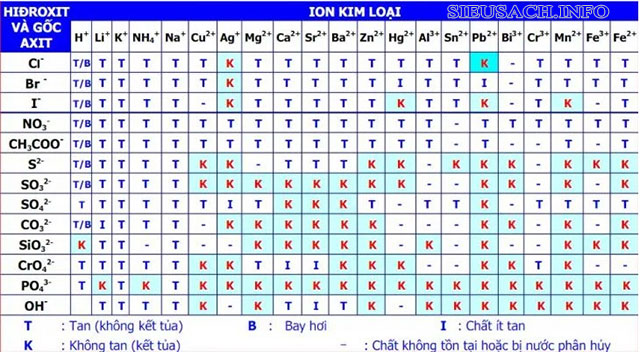
Bảng tính tan của các muối
Muối cacbonat với gốc hóa học là CO3 không tan được trong nước, nhưng muối của các kim loại có tính kiềm như: Li, Na, K,… sẽ tan được trong nước. Và trong bảng tính tan nếu muối được đánh dấu là “t” – biểu thị muối đó có khả năng tan trong nước.
Các muối có gốc silicat (SiO3) và sunfit (SO3) là muối không tan trong nước. Khi kết hợp với các kim loại có tính kiềm thì muối này vẫn có thể tan được trong nước. Vì vậy, trên bảng tính tan, muối của những kim loại này được đánh dấu là “t”.
Tóm lại, các muối được tạo thành từ kim loại kiềm với các gốc khác thì khả năng tan của chúng phụ thuộc vào tính chất của gốc đó và được xác định thông qua bảng tính tan.
Đối với muối gốc Sunfat (SO4) hầu như đều tan trong nước, trừ muối Sunfat của kim loại bari và chì là không tan. Các muối gốc Sunfua (S) đều khó tan trong nước, nhưng trừ những kim loại thuộc vào nhóm I và II trong bảng tuần hoàn hóa học như: BaS, K2S, Na2S, có thể tan trong nước.
Ngoài ra, một số muối không tồn tại hoặc có thể phân hủy ngay trong nước và chúng được ký hiệu là “-” trong bảng tính tan. Tuy nhiên, số lượng của các muối này không nhiều nên bạn có thể dễ dàng học thuộc để tránh nhầm lẫn khi sử dụng bảng tính tan.
Tính tan đối với các bazơ và axit
Các bazơ hầu hết đều không tan trong nước, ngoại trừ các trường hợp là bazơ của kim loại kiềm như: K, Na, Li thì tan trong nước. Còn các kim loại nhóm II như Ca, Ba thì lại ít tan trong nước. Ta có màu của các bazo không tan:
- Cu(OH)2: kết tủa màu xanh lam
- Fe(OH)2: kết tủa màu lục nhạt
- Fe(OH)3: kết tủa màu nâu đỏ
- Mg(OH)2: kết tủa trắng không tan trong kiềm dư
- Riêng các bazo Al(OH)3, Pb(OH)2, Zn(OH)2, Sn(OH)2: kết tủa trắng nhưng sẽ tan trong kiềm dư.
Các hợp chất của axit đều dễ tan trong nước nhưng cũng có trường hợp ngoại lệ: H2CO3 do có liên kết không bền vững nên dễ bị phân hủy trong nước. Bên cạnh đó, hợp chất axit H2SiO3 lại không hề tan trong nước mà ở dạng keo.
Mẹo nhớ bảng tính tan qua bài thơ
Việc ghi nhớ bảng tính tan rất khó giống như bảng hóa trị hay bảng nguyên tử khối. Vì vậy, các bạn học sinh có thể tham khảo bài thơ dưới đây để học thuộc dễ dàng hơn.
Bài thơ học tính tan số 1:
Bazơ, những chú không tan:
Đồng, nhôm, crôm, kẽm, mangan, sắt, chì
Ít tan là của canxi
Magie cũng chẳng điện li dễ dàng.
–
Muối kim loại kiềm đều tan
Cũng như nitrat và “nàng” hữu cơ
Muốn nhớ thì phải làm thơ!
Ta làm thí nghiệm bây giờ thử coi,

Nhớ bảng tính tan qua thơ đơn giản, dễ thuộc
–
Kim koại I (IA), ta biết rồi,
Những kim loại khác ta “moi” ra tìm
Photphat vào nước đứng im (trừ kim loại IA)
Sunfat một số “im lìm trơ trơ”:
Bari, chì với S-r
Ít tan gồm bạc, “chàng khờ” canxi,
–
Còn muối clorua thì
Bạc đành kết tủa, anh chì cố tan (giống Br- và I-)
Muối khác thì nhớ dễ dàng:
Gốc SO3 chẳng tan chút nào! (trừ kim loại IA)
Thế gốc S thì sao? (giống muối CO32-)
Nhôm không tồn tại, chú nào cũng tan
Trừ đồng, thiếc, bạc, mangan, thuỷ ngân, kẽm, sắt không tan cùng chì
–
Đến đây thì đã đủ thi,
Thôi thì chúc bạn trường gì cũng vô!
Bài thơ học tính tan số 2:
Loại muối tan tất cả
là muối ni-tơ-rat
Và muối axetat
Bất kể kim loại nào.
–
Những muối hầu hết tan
Là clorua, sunfat
Trừ bạc, chì clorua
Bari, chì sunfat.
–
Những muối không hòa tan
Cacbonat, photphat
Sunfua và sunfit
Trừ kiềm, amoni.
Thường xuyên làm bài tập và thực hành
Nếu ở trường học có điều kiện thì các em học sinh có thể đến phòng thí nghiệm thường xuyên để thực hành, vận dụng. Bởi bản chất của hóa học là cần nắm vững các phản ứng qua thí nghiệm có thể chứng kiến phản ứng và điều kiện xảy ra.
Việc thực hành nhiều sẽ giúp bạn nhớ và thuộc lòng bảng tính tan cũng như sử dụng chúng. Được trải nghiệm trực tiếp giúp bạn tăng động lực, hứng thú và giúp bảng tính tan trở nên quen thuộc và dễ nhớ hơn. Từ đó những kiến thức lý thuyết sẽ được thực hành trong thực tế giúp bạn ghi nhớ lâu và sâu hơn về bản chất.
Như vậy, bài viết trên đây đã cung cấp và chia sẻ đến bạn những thông tin về bảng tính tan lớp 9. Đây là kiến thức nền tảng trong môn hóa học cần ghi nhớ để các bạn học sinh có thể học tốt môn học này. Đừng quên theo dõi để đón đọc nhiều bài viết hữu ích trên chuthapdoquangninh.org.vn về kiến thức học tập của môn hóa và các môn học khác nhé!




